Le fasi iniziali dell’infiammazione rappresentano un momento fondamentale e integrante del processo di guarigione dopo un trauma muscolo-scheletrico. Interferire con questo fenomeno biologico, bloccandolo in maniera brusca, soprattutto ai suoi esordi, potrebbe portare a risultati di guarigione non ottimali1.
La soppressione dei pathway pro-infiammatori per mezzo di classici farmaci antinfiammatori non steroidei (FANS) è la strategia di norma utilizzata per gestire dolore e infiammazione. Sebbene spesso questi farmaci siano utili per il controllo della sintomatologia algica e di potenziale valore per interrompere il ciclo del dolore, il loro utilizzo protratto o ripetuto potrebbe interferire con i meccanismi di guarigione dei tessuti, promuovere la cronicità e predisporre a un nuovo infortunio. Inoltre, sono noti gli effetti collaterali potenzialmente gravi dei FANS, anche a livello sistemico1.
Per questo motivo, la comunità scientifica ha espresso il suo interesse verso nuove strategie di gestione delle patologie infiammatorie muscolo-scheletriche. Oltre al controllo dei segni e sintomi dell’infiammazione, emerge la necessità della risoluzione dell’infiammazione, e con essa la guarigione del tessuto e accelerazione del recupero funzionale. Numerosi nuovi lavori supportano questo nuovo approccio terapeutico, indicando la necessità di un cambio di paradigma nella gestione del dolore e dell’infiammazione in ambito muscolo-scheletrico 1.
Diversi studi hanno, infatti, dimostrato come molti mediatori che promuovono la fase infiammatoria risultano contemporaneamente imprescindibili per programmare la successiva fase di risoluzione attiva del fenomeno. Dopo una prima fase in cui si osserva una sovraespressione ed una spiccata attività di mediatori molecolari come per esempio PGE2, nei successivi momenti del processo infiammatorio, piccole quantità della stessa PGE2 diventano fondamentali per avviare il processo di riparazione. Infatti, solo se presenti piccole quantità di PGE2 sul “terreno infiammatorio” avverrà un fenomeno cruciale per il processo di guarigione, cioè lo switch dei macrofagi M1 in macrofagi M2, in grado di produrre le molecole di risoluzione e riparazione del tessuto infiammato, note come Specialized Pro-resolving Mediators(SPMs) (lipoxine, protectine, maresine, resolvine)1.
Tra le strategie farmacologiche di gestione della patologia infiammatoria muscolo-scheletrica in grado di indurre i meccanismi pro-risolutivi, il farmaco Traumeel s si è distinto come nuova proposta. Traumeel s, composto da estratti vegetali e minerali diluiti (10-1-10-9), è ampiamente utilizzato per alleviare traumi, infiammazioni e processi degenerativi. Sebbene siano necessari ulteriori approfondimenti per chiarire la modalità d’azione di Traumeel s e dimostrare la relazione causale tra l’inibizione della secrezione di citochine/chemochine in colture cellulari e gli effetti biologici del farmaco, i risultati di alcuni studi in vitro suggeriscono un meccanismo d’azione per gli effetti antinfiammatori osservati nell’uso clinico di Traumeel s2-4.
In particolare, Traumeel s ha dimostrato di agire attraverso meccanismi biologici di down-regolazione di citochine pro-infiammatorie (IL-1β, TNF-α e IL-8) e up-regolazione di citochine antinfiammatorie (IL-10, TGF-β)2,4. Utilizzando un modello murino di peritonite, Jordan e colleghi hanno dimostrato che Traumeel s (denominato nell’articolo Tr14) è in grado di promuovere la biosintesi dei mediatori pro-risolutivi (SPMs) e il reclutamento di leucociti e macrofagi essenziali per la rimozione dei neutrofili polimorfonucleati (PMN) apoptotici e dei detriti cellulari, con outcome positivo sui tempi di risoluzione del danno4.
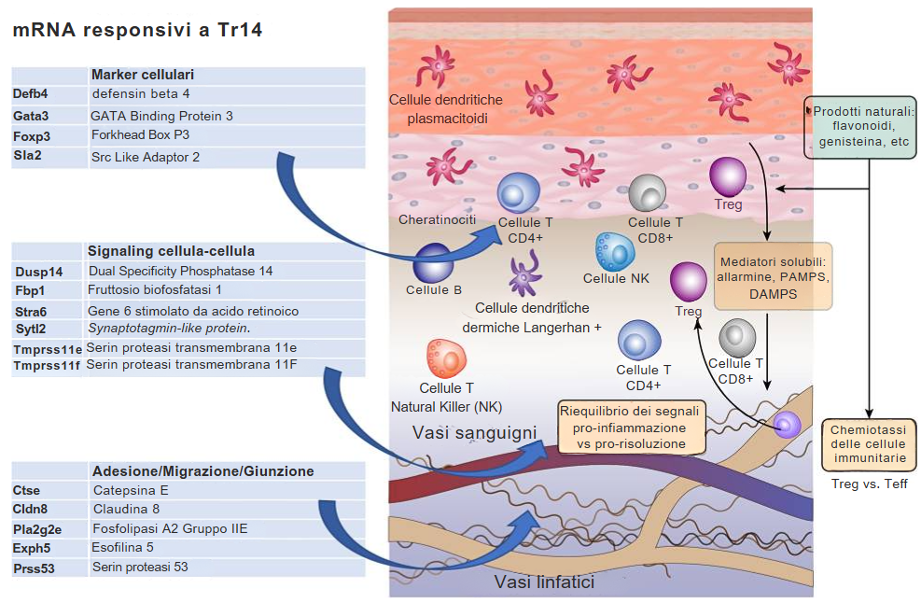
Uno studio di trascrittomica ha permesso di approfondire ulteriormente il meccanismo d’azione di Traumeel s (Tr14), confrontando i suoi effetti rispetto a diclofenac in un modello murino di wound-healing, al fine di identificare pathway antinfiammatori noti o meno3.
Confrontando gli effetti fisiologici dei FANS, come il diclofenac, rispetto alle azioni di Tr14, viene evidenziato come i FANS agiscano attraverso un’inibizione diretta sugli enzimi ciclossigenasi, alterando a valle gli effetti su vasocostrizione/vasodilatazione, coagulazione, chemiotassi e infiammazione. Tr14 non inibisce direttamente gli enzimi COX, consentendo un processo di riparazione delle ferite più naturale, mentre interviene sui livelli di mRNA degli enzimi a valle potenzialmente coinvolti nel processo di risoluzione dell’infiammazione3.
Per ulteriori approfondimenti è possibile consultare la sezione Guna Pro dedicata ai professionisti della salute, al link: https://go.guna.com/Edra
Per domande o per richiedere la visita dell’Informatore Scientifico, è possibile scrivere all’indirizzo info@guna.it
Fonti
- Wolfarth, B., Speed, C., Raymuev, K., Vanden Bossche, L., & Migliore, A. (2022). Managing pain and inflammation associated with musculoskeletal disease: time for a change? Current Medical Research and Opinion, 38(10), 1695–1701. https://doi.org/10.1080/03007995.2022.2108618
- Porozov S, Cahalon L, Weiser M, et al. Inhibition of IL-1beta and TNF-alpha secretion from resting and activated human immunocytes by the homeopathic medication Traumeel S. Clin Dev Immunol. 2004;11(2):143–149.
- St Laurent G, Toma I, Seilheimer B, et al. RNAseq analysis of treatment-dependent signaling changes during inflammation in a mouse cutaneous wound healing model. BMC Genomics. 2021;22(1):854.
- Jordan PM, van Goethem E, Müller AM, et al. The natural combination medicine Traumeel (Tr14) improves resolution of inflammation by promoting the biosynthesis of specialized pro-resolving mediators. 2021;14(11):1123.





