Il Comitato per i Medicinali per Uso umano (Chmp) dell’Agenzia Europea per i Medicinali (Ema) ha raccomandato, nel corso dell’ultimo meeting (11-14 settembre), l’Aic (Autorizzazione all’immissione in commercio) per tredici nuovi farmaci.
Riflettori puntati in particolare per uno dei due biosimilari che hanno ottenuto la raccomandazione. Si tratta Ontruzant (trastuzumab) per il trattamento del cancro al seno precoce e metastatico e del cancro gastrico metastatico. Quest’ultimo è il primo biosimilare di trastuzumab raccomandato per l’approvazione da parte del CHMP. L’anticorpo monoclonale della Samsung Biopes ha dimostrato comparabili qualità, sicurezza ed efficacia del biologico di riferimento Herceptin dell’azienda Roche autorizzato nell’agosto del 2000. Per capire le ricadute basti pensare che nell’ultimo rapporto OsMed dell’Agenzia italiana del Farmaco (Aifa) il trastuzumab risulta il primo principio attivo per incidenza di spesa nell’ambito dell’assistenza ospedaliera con 222,685 milioni di euro.
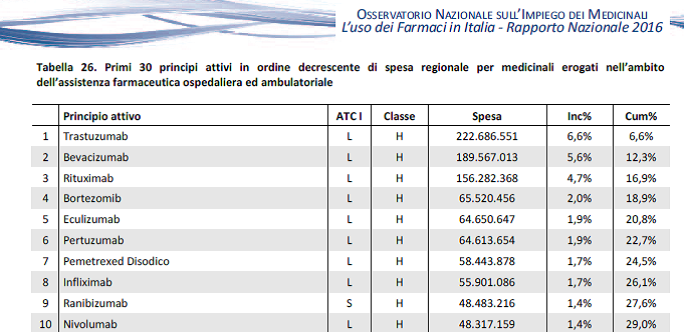
Tornando alla riunione della Chmp oltre ai due biosimilari – il secondo è il Cyltezo (adalimumab) per il trattamento dell’artrite reumatoide, artrite idiopatica giovanile – hanno ottenuto la raccomandazione per la concessione dell’autorizzazione in commercio due antitumorali – Zejula (niraparib), farmaco orfano per il trattamento del cancro ovarico, e Tookad (padeliporfina), per il trattamento dell’adenocarcinoma della prostata – e due medicinali per il trattamento degli adulti con malattia polmonare ostruttiva cronica da moderata a grave – Elecruto Ellipta (fluticasone furoato / umeclidinio / vilanterolo) e Trelegy Ellipta (fluticasone furoato / umeclidinio / vilanterolo). Parere positivo anche per due farmaci ibridi per le persone che fanno uso di oppiacei, Nyxoid (naloxone) e Zubsolv (buprenorfina / naloxone), destinati rispettivamente al trattamento dell’overdose e della dipendenza. Le applicazioni ibride si basano in parte sui risultati di studi e sperimentazioni precliniche effettuate per un prodotto di riferimento e in parte su nuovi dati.
Disco verde anche per il Tremfya (guselkumab), trattamento della psoriasi a placche, e per il VeraSeal (fibrinogeno umano/trombina umana), per l’uso come sigillante durante le operazioni chirurgiche negli adulti, nonché per tre medicinali equivalenti: Imatinib Teva BV (imatinib), per il trattamento della leucemia e dei tumori stromali gastrointestinali; Miglustat Gen.Orph (miglustat), per il trattamento della malattia di Gaucher di tipo 1 da lieve a moderata; Ritonavir Mylan (ritonavir), per l’infezione da HIV.
Infine da segnalare l’estensione delle indicazioni terapeutiche per Benlysta, Tasigna, Firazyr e Stribild.